AUTORES
RUIZ DE CARLOS C.
Residente del Máster de Cirugía Bucal e Implantología. Hospital Virgen de La Paloma. Madrid
ANDRÉS VEIGA M., FERNÁNDEZ-CÁLIZ F. Y MARTÍNEZ-GONZÁLEZ MJS.
Profesores del Máster de Cirugía Bucal e Implantología. Hospital Virgen de La Paloma. Madrid
MARTÍNEZ-GONZÁLEZ JM.
Profesor Titular de Cirugía. Facultad de Odontología. UCM.
RESUMEN
El granuloma periférico de células gigantes (GPCG) es una lesión exofítica poco frecuente de la cavidad oral, también denominada épulis de células gigantes, osteoclastoma, granuloma reparativo de células gigantes o hiperplasia de células gigantes. Se sitúa en la zona gingival y en el hueso alveolar, y es de carácter benigno y de etiología no bien definida.
Se presenta un caso clínico en un paciente varón de 67 años de edad, que presenta una tumoración de base pediculada, localizada en premaxila de 2,5×2 cm, de consistencia blanda, que cubría en su tercio coronal a los dientes 22, 21 y 11, presentaba coloración ligeramente congestiva en su parte superior y algo desplazable.
El tratamiento que se llevó a cabo fue la extirpación completa de la lesión, siendo remitida la pieza para su estudio histopatológico, tras el cual se obtuvo el diagnóstico definitivo de granuloma periférico de células gigantes.
PALABRAS CLAVE
Granuloma periférico de células gigantes; Épulis de células gigantes; Tejidos blandos.
INTRODUCCIÓN
El Granuloma Periférico de Células Gigantes (GPCG), es una tumoración benigna, de carácter inflamatorio crónico que asienta a nivel gingival, pudiendo presentar implicación de los tejidos óseo y periodontal. Se trata de una lesión de partes blandas que rara vez afecta al hueso subyacente, aunque puede llegar a erosionarlo 1-2.
También ha sido denominado tumor periférico de células gigantes, épulis de células gigantes, osteoclastoma, granuloma reparativo de células gigantes e hiperplasia de células gigantes de la mucosa bucal 3.
El GPCG rara vez afecta a la cavidad oral, sin embargo se trata de la lesión de células gigantes que con más frecuencia aparece en los maxilares. Se origina a partir del tejido conjuntivo del periostio o de la membrana periodontal, como respuesta a una irritación local o un traumatismo crónico. Puede aparecer a cualquier edad, con una mayor incidencia entre la quinta y sexta décadas de la vida, con una ligera predilección por el sexo femenino. Tiene mayor preferencia por la mandíbula que por el maxilar y generalmente está localizada en la zona anterior 4-6.
Clínicamente se presenta como un nódulo firme, suave y brillante o como una masa que puede ser sésil o pediculada, pudiendo variar de color, de un rojo oscuro a púrpura o azul; su superficie en ocasiones puede estar ulcerada. El tamaño de estas lesiones varía desde una pequeña pápula a un agrandamiento masivo aunque generalmente son lesiones menores de 2 cm de diámetro, localizadas en la papila interdentaria, en el reborde alveolar edéntulo o en la encía marginal 7.
Se trata de una lesión con crecimiento progresivo, en la mayoría de los casos inducido por un traumatismo de repetición, como la oclusión, en cuyo caso puede llegar a ulcerarse. Es generalmente asintomático, aunque en casos de ulceración superficial de la lesión el paciente puede remitir dolor 7-8.
El tratamiento consiste en la exéresis quirúrgica de la lesión, con un amplio legrado de su base para evitar la aparición de recidivas 9.
El objetivo de la presente publicación es la descripción de un caso de GPCG de 2,5×2 cm de diámetro localizado en la premaxila, y la revisión de la literatura.
CASO CLÍNICO
Paciente varón de 67 años es remitido al Servicio de Cirugía Bucal e Implantología del Hospital Virgen de la Paloma de Madrid, por presentar una tumoración indolora que provoca desplazamiento labial. (Figura 1)
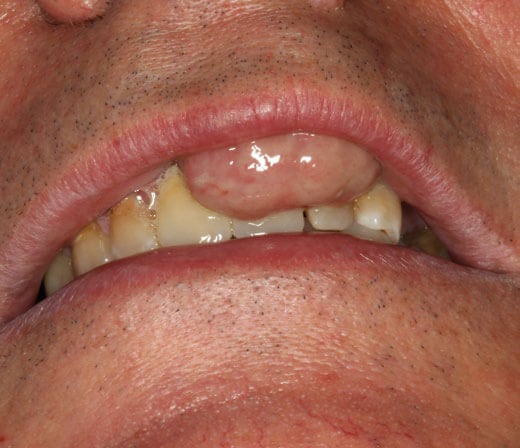
Como antecedentes médicos el paciente padece Diabetes Mellitus tipo II, Hipertensión e Hipercolesterolemia, para lo que se encontraba en tratamiento con Metformina 850 mg 1c/12h, Enalapril 20mg 1c/día y Atorvastatina 20mg/1c/día. No declaró tener alergias y se trató de un paciente exfumador desde hace 1 año de 2 paquetes diarios.
A la exploración intraoral se observó una tumoración de base pediculada, localizada en premaxila de 2,5×2 cm, de consistencia blanda, que cubría en su tercio coronal a los dientes 22, 21 y 11, presentaba coloración ligeramente congestiva en su parte superior y algo desplazable. El resto de la exploración de la cavidad oral se consideró normal. (Figura 2)
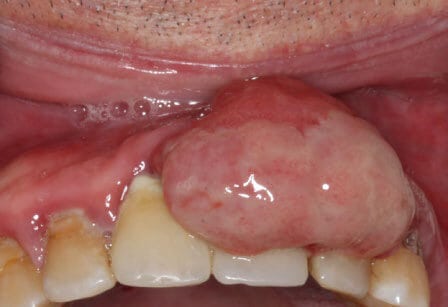
Se informó al paciente sobre el posible diagnóstico de tumoración benigna, solicitando su consentimiento informado para su extirpación y estudio histopatológico. Tras su aprobación, se procedió a la anestesia de la región con una técnica local infiltrativa supraperióstica y perilesional y posterior escisión de la lesión mediante bisturí frío.
Se realizó un colgajo de Newman con despegamiento mucoperióstico de la región de la premaxila y la extirpación total de la lesión tumoral. (Figura 3)
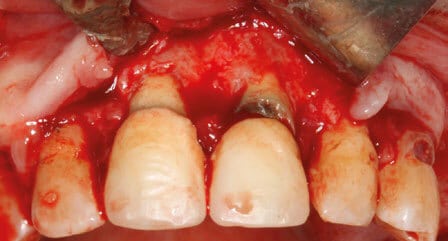
Posteriormente se procedió a la reposición del colgajo mucoperióstico y sutura. (Figura 4)
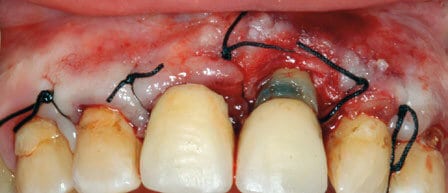
Se prescribió como pautas postoperatorias Amoxicilina 750 mg v.o./8h así como Diclofenaco sódico 50 mg v.o./8h.
Tras 7 días de la intervención y un postoperatorio sin complicaciones se procedió a la retirada de la sutura. (Figura 5)
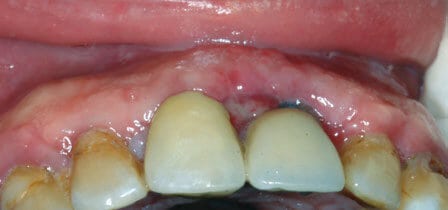
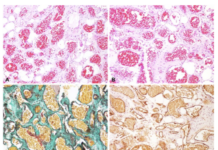
El informe histopatológico informó sobre la presencia de células gigantes con numerosos núcleos y un citoplasma amplio. Estas células, no eran de tipo osteoclasto por lo que el diagnóstico histológico fue de granuloma periférico de células gigantes. (Figura 6)
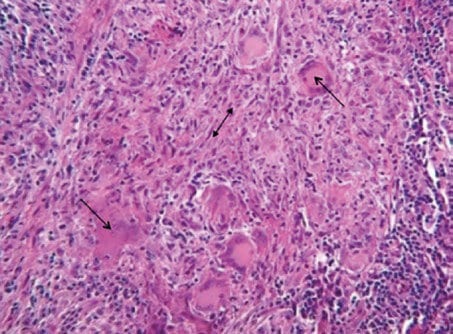
DISCUSIÓN
El GPCG no es una verdadera neoplasia sino una lesión reactiva hiperplásica benigna que supone del 5,1% al 43,6% de las lesiones exofíticas de origen reactivo. Se origina a partir del periostio o de la membrana periodontal tras una irritación o un traumatismo crónico que actúa localmente 9.
Aunque la etiología del GPCG es discutida, muchos autores coinciden en que su origen está en una respuesta proliferativa anormal ante una agresión 3-4. Diversos factores locales se han asociado con este tipo de patología, entre ellos, las exodoncias complicadas, los traumatismos, la presencia de prótesis mal ajusta-das, las restauraciones dentarias desbordantes o rugosas, la impactación de alimentos por malposición dentaria y la presencia de placa bacteriana y cálculo, de la misma manera, se han descrito factores sistémicos que predisponen al aparición de GPCG como en el caso del hiperparatiroidismo 1,10.
En nuestro caso, el paciente presentaba coronas metal-cerámica mal ajustadas en los dientes 22 y 11, así como una higiene bucal deficiente.
La mayoría de los autores consultados coinciden en que se presenta con más frecuencia en mujeres que en hombres; sin embargo, Chaparro-Avendaño y cols 3., observaron una pequeña predilección por el sexo masculino, lo que coincide con el caso descrito anteriormente, en el que el paciente es varón.
Tiene una prevalencia ligeramente mayor en el grupo de edad comprendida entre los 30 y 70 años 11, como en el caso presentado, aunque hay autores que sitúan su máxima incidencia por debajo de los 30 años de edad 9. Se han descrito casos de GPCG en niños, donde se trata de lesiones más agresivas, con reabsorción de la cresta alveolar interproximal, desplazamiento de los dientes adyacentes y múltiples recidivas 4,6, como ocurre en los casos descritos por Volpato y cols 5., y Nekouei y cols 6., que describen casos de GPCG en pacientes de 4 años de edad, o el descrito por Abu Gharbyah y cols 12., en el que la paciente tenía 23 años.
En cuanto a la localización, la literatura consultada coincide en que es más común encontrarlos en la mandíbula que en el maxilar, variando la proporción de 2,4:1 a 1,6:1 según los distintos autores, y dentro de la mandíbula, la ubicación más común es la región premolar y molar, aunque hay autores que sugieren que es más frecuente encontrarlos en la zona incisiva-canina 3,9,13. En nuestro caso, el paciente presentaba la lesión en la zona anterior del maxilar.
Las lesiones pueden estar relacionadas con los dientes, en zonas edéntulas o junto a implantes dentales. En el estudio realizado por Lester y cols 1., en 242 pacientes, 203 estaban relacionados con dientes, 34 se encontraban en zonas edéntulas y 5 en relación con implantes.
Haciendo referencia a la clínica del GPCG; las lesiones se presentan como un nódulo firme, sésil o pediculado, con una coloración rojiza, morada, azulada, rosada, blanca, marrón o una combinación de estas, con una consistencia blanda; puede tener la superficie ulcerada, y generalmente es asintomática. En cuanto al tamaño, las lesiones generalmente no sobrepasan los 2 cm de diámetro y en la mayoría de los casos el crecimiento es inducido por traumatismos repetidos 1,6-7,10.
En el caso descrito anteriormente, el aspecto de la lesión coincide con el establecido por la literatura consultada, sin embargo, el tamaño de la lesión supera la media, ya que se trató de una lesión de 2,5×2 cm de diámetro.
La afectación ósea está en relación con el tiempo de evolución; es más extensa a medida que aumenta dicho tiempo, a diferencia del GCCG que, por el contrario, asienta en el hueso desde un primer momento, y puede afectar a los tejidos blandos en el curso de su evolución 9,14-15. Por este motivo, es imprescindible una radiografía para distinguir ambas lesiones 13.
Debido a que la apariencia clínica de GPCC es similar a la del GCCG, el fibroma, el fibroma osificante periférico y el granuloma piógeno, se requiere el diagnóstico mediante el estudio histopatológico de la lesión 4,16.
Histológicamente, el GPCC se compone de nódulos de células gigantes multinucleadas en un fondo de células mesenquimáticas ovoides y fusiformes y glóbulos rojos extravasados. Las células gigantes pueden contener solo unos pocos núcleos o hasta varias docenas de ellos. Algunos de ellos son grandes núcleos vesiculares; otros muestran pequeños núcleos picnóticos. El origen de la célula gigante es desconocido. Estudios ultraestructurales e inmunológicos han demostrado que las células gigantes derivan de los osteoclastos 3,8, aunque según Sargolzaei y cols 16., derivan de los histiocitos/macrófagos. Por otro lado, Kumar y cols 17., sugiere que estos macrófagos pueden regular la angiongénesis en los granulomas de células gigantes (tanto de los periféricos como de los centrales), y dicha angiogénesis tiene un papel importante en el comportamiento clínico de la lesión.
El tratamiento del GPCG consiste en la exéresis quirúrgica eliminando toda la base de la lesión para evitar recidivas, así como la supresión de los factores etiológicos una vez identificados. La mayor parte de las lesiones responden satisfactoriamente al legrado quirúrgico minucioso. Cuando está afectada la membrana periodontal puede ser necesaria la extracción de los dientes adyacentes para conseguir una extirpación completa, aunque inicialmente esté contraindicada la exodoncia 3,5-9.
Existe otra opción de tratamiento que consiste en la inyección de Oleato de Etanolamina (OE), que está indicada para los casos de GPCG recurrentes tras la extirpación quirúrgica que exigen un legrado más agresivo o la extracción de los dientes afectados. Este tratamiento ofrece una alternativa a los tratamientos convencionales como la cirugía, el curetaje, la electrodesecación y la cirugía láser, mediante un procedimiento sencillo, seguro, de bajo coste y generalmente bien tolerado por el paciente, con una alta tasa de éxito y una baja probabilidad de recurrencia 18.
En cuanto a la recidiva del GPCG podemos decir que es rara, presentándose entre un 1,39% a un 11% según diferentes autores 3,7,13. Un punto que cabe destacar es la alta tasa de recurrencia que existe en las lesiones adyacentes a implantes dentales y además parece tener una naturaleza más agresiva 19-20. En el estudio de Les-ter y cols 1., 2 de los 5 casos de GPCG sobre implantes (40%) tuvieron recurrencias múltiples, mientras que 6 de 237 casos de GPCG no relacionados con implantes (2,5%) tuvieron dichas recurrencias.
En el caso que presentamos no se apreció recidiva tras 4 años.
CONCLUSIONES
El diagnóstico temprano y preciso de GPCG permite un manejo conservador con un menor riesgo de comprometer los dientes y el hueso adyacente, y para ello es imprescindible su estudio histopatológico. ●
BIBLIOGRAFÍA
- Lester SR, Cordell KG, Rosebush MS, Palaiologou AA, Maney P. Peripheral giant cell granulomas: a series of 279 cases. Oral Surg Oral Med Oral Pathol Oral Radiol. 2014;118(4):475-82.
- Brown AL, Camargo de Moraes P, Sperandio M, Borges Soares A, Araújo VC, Passador-Santos F. Peripheral giant cell granuloma associated with a dental implant: a case report and review of the literature. Case Rep Dent. 2015; 697673.
- Chaparro-Avendaño AV, Berini-Aytés L, Gay Escoda C. Granuloma periférico de células gigantes. A propósito de 5 casos y revisión de la literatura. Med Oral Patol Oral Car Bucal 2005;10:48-57.
- DaSilva FC, Piazzetta CM, Torres-Pereira CC, Schussel JL, Amenábar JM. Gingival proliferative lesions in children and adolescents in Brazil: A 15-year-period cross-sectional study. J Indian Soc Periodontol. 2016;20(1):63-6.
- Volpato LE, Leite CA, Anhesini BH, Aguilera JM, Borges ÁH. Peripheral Giant Cell Granuloma in a Child Associated with Ectopic Eruption and Traumatic Habit with Control of Four Years. Case Rep Dent 2016; 6725913.
- Nekouei A, Eshghi A, Jafarnejadi P, Enshaei Z. A Review and Report of Peripheral Giant Cell Granuloma in a 4-Year-Old Child. Case Rep Dent. 2016; 7536304.
- Rodrigues SV, Mitra DK, Pawar SD, Vijayakar HN. Peripheral giant cell granuloma: This enormity is a rarity. J Indian Soc Periodontol. 2015;19(4):466-9.
- Tandon PN, Gupta SK, Gupta DS, Jurel SK, Saraswat A. Granuloma periférico de células gigantes. Contemp Clin Dent . 2012; 3(1): S118-S121.
- Vázquez Piñeiro MT, González Bereijo JM, Niembro de Rasche E. Granuloma periférico de células gigantes: caso clínico y revisión de la literatura. RCOE 2002;7(2): 201-6.
- Choi C, Terzian E, Schneider R, Trochesset DA. Peripheral giant cell granuloma associated with hyperparathyroidism secondary to end-stage renal disease: a case report. J Oral Maxillofac Surg. 2008;66(5):1063-6.
- S Falaschini, Ciavarella D, Mazzanti R, Di Cosola M, Turco M, Escudero N et al . Granuloma periférico de células gigantes: análisis inmunohistoquímico de la población celular en tres casos clínicos. Av Odontoestomatol 2007;23(4): 181-8.
- Abu Gharbyah AZ, Assaf M. Management of a Peripheral Giant Cell Granuloma in the esthetic area of upper jaw: A case report. Int J Surg Case Rep. 2014;5(11):779-82.
- Shadman N, Ebrahimi SF, Jafari S, Eslami M. Peripheral Giant Cell Granuloma: A Review of 123 Cases. Dent Res J. 2009;6(1):47-50.
- Duque Serna FL, Franco Lina M, Ardila Medina CM. Granuloma central de células gigantes: presentación de diez casos. AMC 2012;16(5): 628-36.
- Zargaran M, Moghimbeigi A, Afsharmoghadam N, Nasr Isfahani M, Hashemi A. A Comparative Study of Cathepsin D Expression in Peripheral and Central Giant Cell Granuloma of the Jaws by Immunohistochemistry Technique. J Dent (Shiraz). 2016;17(2):98-104.
- Sargolzaei S, Taghavi N, Poursafar F. Are CD68 and Factor VIII-RA Expression Different in Central and Peripheral Giant Cell Granuloma of Jaw: An Immunohistochemical Comparative Study. Turk Patoloji Derg 2017;1(1):1-8.
- Kumar VV, Krishanappa SJ, Prakash SG, Channabasaviah GH, Murgod S, Pujari R et al. Quantification and Correlation of Angiogenesis with Macrophages by Histomorphometric Method in Central and Peripheral Giant Cell Granuloma: An Immunohistochemical Analysis. J Clin Diagn Res. 2016;10(3):ZC01-5.
- Said Ahmed W. Efficacy of Ethanolamine Oleate Sclerotherapy in Treatment of Peripheral Giant Cell Granuloma. J Oral Maxillofac Surg. 2016;74(11):2200-6.
- Jané-Salas E, Albuquerque R, Font-Muñoz A, González-Navarro B, Estrugo Devesa A, López-López J. Pyogenic Granuloma/Peripheral Giant-Cell Granuloma Associated with Implants. Int J Dent. 2015; 839032.
- Pacifici A, Carbone D, Marini R, Sfasciotti GL, Pacifici L. Clinical Management of a Peri-Implant Giant Cell Granuloma. Case Rep Dent. 2015; 976756.